Ley de Gay-Lussac - Ejercicios Resueltos

Qué hay amigos, hoy hablaremos sobre otra ley muy importante en los gases y que de manera resumida y muy práctica la vamos a ver durante este post, así que toma asiento, cuaderno, lapicero y calculadora en mano que es momento de aprender algo nuevo, y eso algo nuevo es ni nada más ni nada menos que sobre la ley de gay-lussac .
bien, hasta este momento en el blog tenemos dos leyes relacionadas entre si que dan paso a ley general del estado gaseoso que se verá en otro post, por ahora ya se ha comprendido de que trata la ley de charles y la ley de boyle-mariotte y si no las has revisado pues no esperes más, y dales una checadita.
Entendiendo la Ley de Gay-Lussac
Vamos a lo que nos importa e interesa, esta ley tiene una particularidad en general al igual que las demás, por ejemplo; en la ley de charles la presión permanece constante, en la ley de boyle-mariotte es la temperatura quien permanece constante y para finalizar en la la ley de Gay-Lussac es el volumen quien permanece constante.
Antes de meternos en las matemáticas y fórmula de gay-lussac, veremos algo más sobre esta ley.
Aquí entenderemos porque la presión y temperatura van muy de la mano y son totalmente proporcionales, es decir, supongamos que acabas de comprar un aerosol, si sometemos ese aerosol a cierta temperatura de tal manera que aumente, la presión también aumentará, a esta relación se le llama proporcionalidad.

Notables científicos, físicos y químicos dedicaron parte de su tiempo para poder entender mejor esta ley, pero fue Gay-Lussac un físico-químico de origen Francés, que estudió a fondo el comportamiento de los gases respecto a la relación entre la presión y la temperatura, su ley estable lo siguiente.
Ahora si, vamos a lo matemático.
Fórmula de Gay-Lussac
Como dijimos texto atrás, la proporcionalidad que existe en esta ley es sobre la presión y la temperatura, matemáticamente colocaremos esto como:
$\displaystyle P\propto T$
Ahora introduzcamos una constante de proporcionalidad esto da paso a que se vea de la siguiente forma, es como un despeje simple.
$\displaystyle \frac{P}{T}=k$
Ahora al tratarse de una igualdad, podemos considerar las condiciones inicial y final, quedando la ecuación o fórmula matemática de la Ley de Gay-Lussac de la siguiente forma:
$\displaystyle \frac{{{P}_{1}}}{{{T}_{1}}}=\frac{{{P}_{2}}}{{{T}_{2}}}$
donde:
$\displaystyle {{P}_{1}}=$ Presión Inicial
$\displaystyle {{T}_{1}}=$ Temperatura Inicial
$\displaystyle {{P}_{2}}=$ Presión Final
$\displaystyle {{T}_{2}}=$ Temperatura Final
Gráfica de la Ley de Gay-Lussac
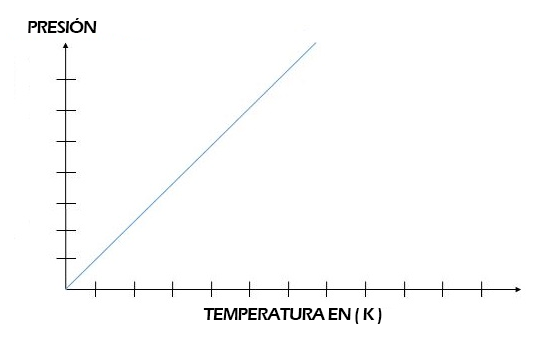
En la gráfica podremos observar claramente la proporcionalidad entre la presión y la temperatura, recordemos también que para las condiciones de un gas, las temperaturas deben darse en grados Kelvin.
Ejemplos resueltos de la Ley de Gay-Lussac
Solución: Si leemos detalladamente el problema nos podremos dar cuenta que las condiciones iniciales de temperatura y presión nos las dan como datos, al igual que la presión final, pero el único dato que no nos dan es la temperatura final, y la cual nos piden en °C.
Vamos a colocar nuestros datos:
$\displaystyle {{P}_{1}}=$ 440 mm de Hg.
$\displaystyle {{T}_{1}}=$ 35°C + 273 = 308 °K
$\displaystyle {{P}_{2}}=$ 760 mm de Hg.
$\displaystyle {{T}_{2}}=$ ?
He sumado a 35° la cantidad de 273, para poder hacer la conversión a grados Kelvin. Es muy importante que lo conviertan sino no dará el resultado que esperamos.
Ahora, usamos la fórmula para esta ley, la cual colocaré de nuevo.
$\displaystyle \frac{{{P}_{1}}}{{{T}_{1}}}=\frac{{{P}_{2}}}{{{T}_{2}}}$
Despejando a $\displaystyle {{T}_{2}}$
Nos queda
$\displaystyle {{T}_{2}}=\frac{{{P}_{2}}{{T}_{1}}}{{{P}_{1}}}$
Ahora sustituimos nuestros datos.
$\displaystyle {{T}_{2}}=\frac{(760mmdeHg)(308{}^\circ K)}{440mmdeHg}=532{}^\circ K$
Pero nos piden el resultado en °C, por lo que restaremos 273 a la cantidad resultante en grados Kelvin.
$\displaystyle {{T}_{2}}=532{}^\circ K-273=259{}^\circ C$
Como podemos observar en las condiciones iniciales del problema, la temperatura aumentó y como resultado también la presión, esto quiere decir que hemos resuelto el problema con éxito.
Veamos otro ejemplo:
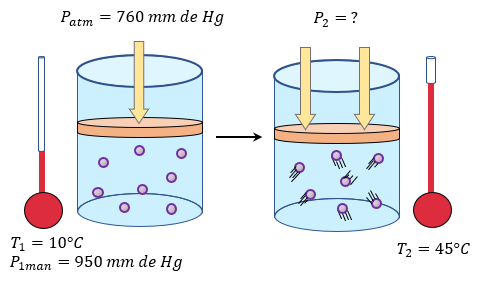
Solución: Para este ejemplo podemos observar claramente que la variable que nos hace alta es la presión final, por lo que haremos una recopilación de nuestros datos y empezar a resolver.
Si hacemos el análisis también nos damos cuenta que la temperatura ha aumentado de 45°C a 125°C esto quiere decir que por la proporcionalidad que existe entre la presión y temperatura, la presión aumentará como resultado final, no sabemos en que cantidad, pero si sabemos que aumentará.
¡Muy importante! y vuelvo a repetirlo, la temperatura siempre será en escala absoluta, es decir grados Kelvin.
Datos:
$\displaystyle {{P}_{1}}=$ 460 mm de Hg.
$\displaystyle {{T}_{1}}=$ 45°C + 273 = 318 °K
$\displaystyle {{P}_{2}}=$ ?
$\displaystyle {{T}_{2}}=$ 125°C + 273 =398°K
Por fórmula tenemos
$\displaystyle \frac{{{P}_{1}}}{{{T}_{1}}}=\frac{{{P}_{2}}}{{{T}_{2}}}$
Despejando $\displaystyle {{P}_{2}}$
Nos queda
$\displaystyle {{P}_{2}}=\frac{{{P}_{1}}{{T}_{2}}}{{{T}_{1}}}$
Reemplazando nuestros datos en la fórmula
$\displaystyle {{P}_{2}}=\frac{(460mmdeHg)(398{}^\circ K)}{318{}^\circ K}=575.72mmdeHg$
Pero, para entenderlo mejor sigamos viendo un tercer ejemplo más 😎
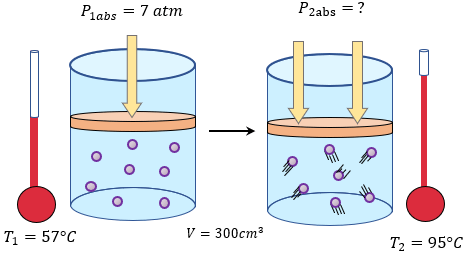
Solución: Anotemos los datos de nuestro problema y veamos las variables que tenemos y la que nos hace falta, recordemos mantener a la temperatura en su escala absoluta, por lo que tenemos que convertir a Kelvin.
$\displaystyle {{P}_{1}}=2atm$
$\displaystyle {{T}_{1}}=27{}^\circ C$
$\displaystyle {{P}_{2}}=3atm$
$\displaystyle {{T}_{2}}=?$
Convertimos a la temperatura 1, en absoluta, quedando así:
$\displaystyle {{T}_{1}}=27+273=300{}^\circ K$
Ahora, nos damos cuenta que nos hace falta la temperatura final, o T2, por lo que procedemos a realizar el despeje de la fórmula.
$\displaystyle {{T}_{2}}=\frac{{{P}_{2}}{{T}_{1}}}{{{P}_{1}}}$
Sustituyendo en nuestros datos:
$\displaystyle {{T}_{2}}=\frac{{{P}_{2}}{{T}_{1}}}{{{P}_{1}}}=\frac{(3atm)(300{}^\circ K)}{2atm}=450{}^\circ K$
Por lo que la temperatura aumentó a 450°K, por lo que tiene lógica, ya que si vemos el aumento de la temperatura, se debe al aumento de la presión.
Solución: Nuevamente debemos recopilar nuestros datos, y a su vez recordar en convertir la temperatura que está en Celcius y pasarlas a Kelvin, así que aquí vamos.
$\displaystyle {{P}_{1}}=4atm$
$\displaystyle {{T}_{1}}={{47}^{{}^\circ }}C$
$\displaystyle {{P}_{2}}=?$
$\displaystyle {{T}_{2}}=127{}^\circ C$
Pasando a temperatura absoluta a nuestras temperaturas tenemos que:
$\displaystyle {{T}_{1}}=47+273=320{}^\circ K$
$\displaystyle {{T}_{2}}=127+273=400{}^\circ K$
Ahora despejamos de nuestra fórmula a la presión final o P2.
$\displaystyle {{P}_{2}}=\frac{{{P}_{1}}{{T}_{2}}}{{{T}_{1}}}=\frac{(4atm)(400{}^\circ K)}{320{}^\circ K}=5atm$
Por lo que la presión final es de 5 atmósferas ¿complicado?, seguro que no, no es complicado. Recuerda practicar y resolver más ejercicios para que aprendas de una vez por todas. 😎
? Ejercicios para Practicar de Gay - Lussac
Resuelva los siguientes ejercicios y compruebe los resultados paso a paso haciendo click en la parte “ver solución”. ??
-
AGRADESCO QUE LEAS MIS COMENTARIOS
★★★★★
-
hola gracias por tu trabajo pero en la parte donde hay que cambiar Celsius a kelvin la formula exacta es:
°C + 273,15 no °C + 273 (solo para aclarar)
y el segundo error es que grados kelvin no lleva el símbolo grado ° debido a que K es una escala absoluta,entonces es:
K no °K
★★★★★
-
estoy es perando que contesten a sus aclaraciones el tien toda la razon
★★★★★
-
-
muy buena la información de los diversos temas, y lo mejor es que presente ejercicios muy prácticos Felicitaciones.
-
un gas se encuentra en un recipiente cerrado, pasa de encontrarse a 15 atm de presión a 16 atm.¿cuál será la temperatura final dentro del recipiente si al principio se medían 25° c?
171 Deja tu comentario
Deja una respuesta

Estos temas te pueden interesar